«Спутник V» прошел этап научной консультации регулятора ЕС
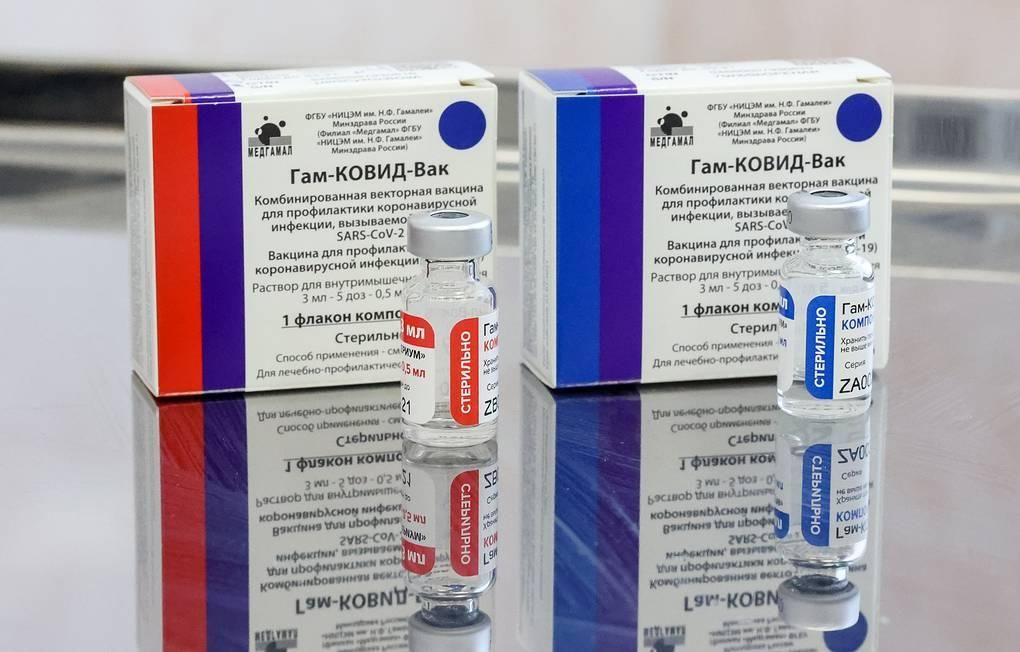
Европейское агентство по лекарственным средствам (ЕМА) завершило консультирование разработчика российской вакцины от коронавируса «Спутник V», теперь возможна подача заявки на регистрацию на рынке ЕС.
«На данном этапе мы можем сказать, что Национальный исследовательский центр эпидемиологии и микробиологии имени Гамалеи получил научную консультацию от ЕМА по разработке их вакцины для предотвращения COVID-19 «Спутник V» (также известной как Gam-COVID-Vac). … В качестве следующего шага компания может подготовить заявку на получение регистрационного удостоверения (marketing authorisation)», – сообщили в агентстве, передает ВЗГЛЯД со ссылкой на РИА «Новости».
Там пояснили, что процесс научного консультирования хорошо отлажен в ЕМА и доступен всем компаниям, чтобы облегчить подготовку их программы разработки. Представитель ЕМА добавил, что агентство пока не получило заявку от разработчика «Спутник V», сроки получения одобрения для рынка ЕС от ЕМА можно будет обсуждать после поступления такой заявки. В случае выдачи условного регистрационного удостоверения и одобрения со стороны Еврокомиссии, российская вакцина сможет централизованно поставляться в ЕС.
В настоящее время на рынке Евросоюза авторизованы вакцины компаний Pfizer/BioNTech (закупка до 600 млн доз), Moderna (160 млн доз) и AstraZeneca (до 400 млн доз). Кроме того, ЕК заключила контракты на поставки в ЕС вакцин с компаниями Johnson&Johnson, Sanofi-GSK, CureVac. До настоящего момента эти разработчики еще не подали заявки для авторизации своих препаратов на рынке ЕС, но в ближайшее время ожидается подача заявки от J&J.
Ранее в США «Спутник V» признали одним из крупнейших прорывов России со времен СССР. Перед этим научный журнал Lancet опубликовал результаты третьей фазы клинических исследований вакцины «Спутник V», подтверждающие ее высокую эффективность и безопасность.
Тем временем в РФПИ допустили возможность одобрения российской вакцины против коронавируса «Спутник V» Европейским агентством по лекарственным препаратам (EMA) в феврале – начале марта.
